Його існування — лише думковий експеримент, проте наслідки для науки виявилися цілком реальними: цей «демон» змусив учених переосмислити поняття ентропії, енергії, порядку та інформації — основи не лише фізики, а й хімії.
Як народився демон
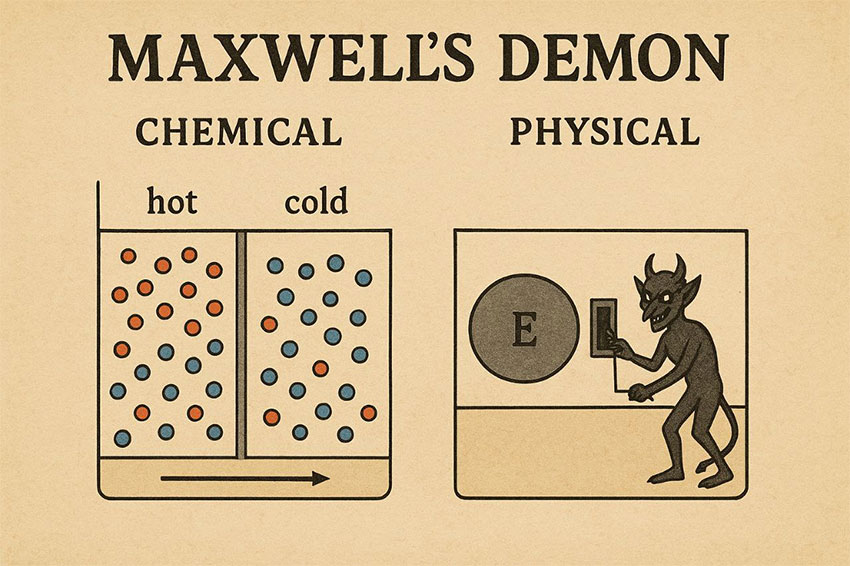
У 1867 році шотландський фізик Джеймс Клерк Максвелл — один із творців електродинаміки — запропонував парадоксальну ідею. Він уявив істоту, здатну розрізняти окремі молекули газу в посудині, розділеній перегородкою з маленьким отвором.
Якщо молекула рухається швидко — демон відкриває заслінку й пропускає її в один бік. Якщо повільно — не пускає. Через деякий час у лівій половині газ охолоджується, у правій нагрівається. Виходить, що частина системи стає «упорядкованішою» без витрати енергії — ніби створюється машина, яка порушує другий закон термодинаміки, адже ентропія ізольованої системи начебто зменшується.
Другий закон і хімічний світ
Другий закон термодинаміки — це закон, що керує усіма змінами в природі. У хімії він визначає, в який бік піде реакція, чи буде процес самодовільним, чи ні. Якщо енергія системи розподіляється рівномірно, ентропія зростає — і процес триває сам собою.
Наприклад:
При змішуванні газів, скажімо, водню та кисню, молекули хаотично перемішуються — ентропія збільшується.
При розчиненні кухонної солі у воді йони Na⁺ та Cl⁻ залишають кристалічну решітку і рухаються вільно між молекулами води — теж збільшення безладдя.
Навіть аромат кави, що розповсюджується кімнатою, — прояв другого закону: молекули летючих речовин дифундують, досягаючи термодинамічної рівноваги.
Отже, усе навколо нас «прагне» до стану більшої ентропії, тобто більшого хаосу. І тільки витрати енергії дозволяють створювати порядок — у хімічних реакціях, у кристалах, у живих клітинах.
Ентропія на мові молекул
Ентропію часто уявляють як абстрактну величину, але в хімії її можна буквально «побачити». Вона зростає, коли збільшується кількість способів, якими можуть розміститися або рухатися частинки системи.
У реакції 2H₂ + O₂ → 2H₂O ентропія зменшується, бо з трьох молекул газу утворюються дві молекули пари. Проте виділяється велика кількість енергії — тепло компенсує втрату ентропії.
Навпаки, у реакції розкладу CaCO₃ → CaO + CO₂ ентропія зростає, адже утворюється газ із твердого тіла.
Демон Максвелла у цьому сенсі — метафора спроби втрутитися в цей природний баланс: відсортувати частинки, змусити природу працювати «безкоштовно».
Інформація як енергія
Парадокс Максвелла змусив учених шукати, де саме приховано ціну впорядкування. У 1929 році Лео Сцілард довів, що демон повинен збирати інформацію про кожну молекулу — її швидкість, положення, напрямок руху. А отримання та зберігання цієї інформації теж вимагає енергії.
Згодом Рольф Ландауер сформулював закон: стираючи інформацію, система виділяє тепло. Отже, навіть якщо демон тимчасово створює порядок, він неминуче підвищує ентропію навколишнього середовища. Закон не порушено — лише розширено його зміст: інформація теж має енергетичну ціну.
Хімічні демони навколо нас
Якщо придивитися, у хімічному світі повно «демонів Максвелла».
Ферменти — білкові каталізатори в організмах — «відбирають» потрібні молекули з мільйонів інших. Вони знижують енергетичний бар’єр реакцій, спрямовуючи їх у потрібний бік. Але підтримка структури ферментів вимагає енергії — живі клітини платять за цей «інтелектуальний відбір».
Мембрани клітин — своєрідні бар’єри з «заслінками». Іонні канали пропускають лише певні йони (Na⁺, K⁺, Ca²⁺), підтримуючи електричний потенціал. Цей процес вражаюче нагадує роботу демона Максвелла — контроль руху частинок з одного боку на інший.
Кристалізація — ще один приклад тимчасового зменшення ентропії. З хаотичних молекул розчину утворюється впорядкована решітка. Але щоб це сталося, система повинна віддати енергію (тепло), компенсуючи втрату ентропії.
Усі ці приклади показують: природа постійно «грає» з другим законом, створюючи локальний порядок за рахунок глобального хаосу.
Демон у сучасній фізико-хімії
У ХХІ столітті ідеї демона Максвелла оживають у нанохімії, біофізиці та інформаційній термодинаміці. Вчені створюють мікроскопічні пристрої, які справді можуть керувати окремими молекулами.
У дослідах із лазерними пінцетами частинки утримуються й пересуваються за допомогою сфокусованого світла. Дослідники фіксують теплові флуктуації, «виловлюючи» найбільш енергетичні стани — буквально як демон у моделі Максвелла. А у хімічних реакціях на нанорівні подібні принципи реалізуються в молекулярних машинах, здатних керувати напрямком реакцій завдяки зовнішнім сигналам (світло, електричне поле).
Філософський вимір
Демон Максвелла став не лише науковим, а й філософським образом — символом межі між хаосом і порядком, знанням і енергією. Він показав, що навіть думка про впорядкування системи має фізичну ціну.
Сучасна хімія і біологія фактично живуть завдяки «демонам» — системам, що підтримують порядок усередині себе, сплачуючи енергією, яку отримують із зовні. Живі організми, клітини, навіть мозок людини — це демони Максвелла, що обмінюють інформацію на зменшення локального хаосу.
Демон Максвелла — не спроба порушити закони природи, а елегантна метафора того, як у Всесвіті взаємодіють енергія, інформація та порядок. Його історія з’єднала фізику й хімію, показавши: будь-яке створення порядку — від синтезу кристалів до мислення — коштує енергії.
І можливо, головний урок демона полягає в тому, що життя саме по собі є найбільшою антиентропійною системою. Ми всі — демони Максвелла, які, використовуючи знання, підтримують свій маленький порядок у безмежному хаосі Всесвіту.
Список використаної літератури
- Szilard L. On the decrease of entropy in a thermodynamic system by the intervention of intelligent beings // Behavioral Science. — 1964. — Vol. 9, No. 4. — P. 301–310.
- Landauer R. Information is physical // Physics Today. — 1991. — Vol. 44, No. 5. — P. 23–29. DOI: 10.1063/1.881299
- Bennett C. H. Notes on Landauer’s principle, reversible computation and Maxwell’s demon // Studies in History and Philosophy of Modern Physics. — 2003. — Vol. 34, No. 3. — P. 501–510. DOI: 10.1016/S1355-2198(03)00039-X
- Rex A. Maxwell’s Demon — A Historical Review // Entropy. — 2017. — Vol. 19, No. 6. — Article 240. DOI: 10.3390/e19060240
- Toyabe S., Sagawa T., Ueda M., Muneyuki E., Sano M. Information heat engine: converting information to energy by feedback control // Nature Physics. — 2010. — Vol. 6. — P. 988–992. DOI: 10.1038/nphys1821
- Sagawa T. Second law, entropy production, and reversibility in thermodynamics of information // arXiv preprint. — 2017. — arXiv:1712.06858
- Parrondo J. M. R., Horowitz J. M., Sagawa T. Thermodynamics of information // Nature Physics. — 2015. — Vol. 11. — P. 131–139. DOI: 10.1038/nphys3230
Вікторія Носач, аспірантка та викладачка кафедри хімії Національного університету «Києво-Могилянська Академія»,
інженерка Наукового інституту фізичної хімії ім. Л.В. Писаржевського НАН України




















 Засновник та видавець
Засновник та видавець