Хіміки не були б самими собою якби не знайшли обхідний шлях до того як «побачити» молекули. На перший погляд це може здатися магією, але насправді йдеться про точні фізичні методи, що дозволяють «почути» відповідь молекули на правильно поставлене запитання: світло, магнітне поле або потік енергії. Відповідями на ці запитання є спектри – впорядковані сигнали, які потрібно навчитися читати. Під час навчання ця задача часто може спрощуватись до аналізу окремого спектра щоб полегшити процес опанування методики роботи з тим чи іншим методом та набуття відповідних навичок. Однак, жоден спектроскопічний метод не є самодостатнім і повноцінне встановлення структури органічної сполуки завжди ґрунтується на комплексному підході, де кожен метод дає фрагмент інформації, а остаточний висновок є результатом їх логічного поєднання. Фактично хіміки збирають докупи частинки пазлу щоб отримати повноцінну картину.
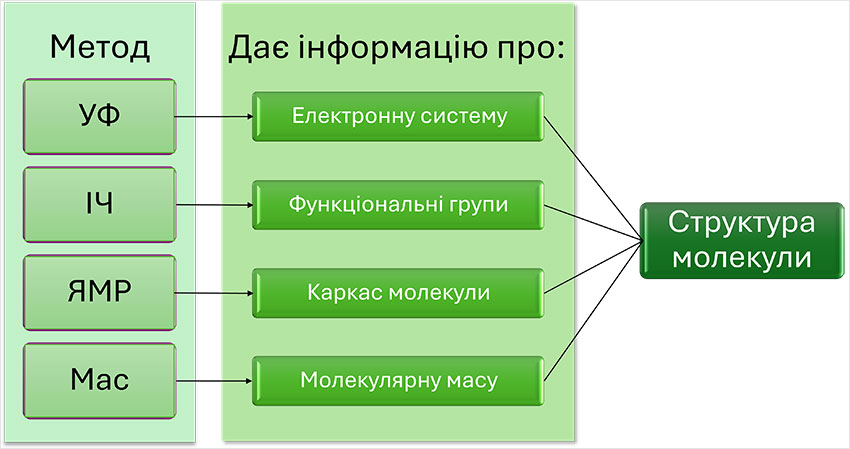
То що ж таке ті загадкові спектри? На перший погляд будь-який спектр виглядає як графік із піками, однак варто придивитися ближче і ви побачите, що їх вигляд залежно від методу одержання значно відрізняється. Спектр є результатом взаємодії молекули з певним видом енергії. Кожен сигнал у спектрі несе певну фізико-хімічну інформацію, яка має бути правильно розшифрована та співвіднесена з молекулярною будовою досліджуваної сполуки. Різні методи дозволяють отримати різні фрагменти цієї інформації, тому справжній структурний аналіз завжди схожий на складання пазла.
УФ-спектроскопія: електронна система та кількісний аналіз
Одним із найперших та найпростіших для розуміння методів є ультрафіолетова спектроскопія (УФ), що базується на поглинанні електромагнітного випромінювання, яке викликає електронні переходи в молекулі. Якщо простіше, то деякі органічні молекули здатні поглинати світло певної енергії. Це відбувається тоді, коли електрони в системах подвійних зв’язків або спряжених фрагментах можуть переходити на вищий енергетичний рівень. Саме тому ароматичні сполуки, барвники або молекули з розвиненою π-системою мають характерні спектри поглинання.
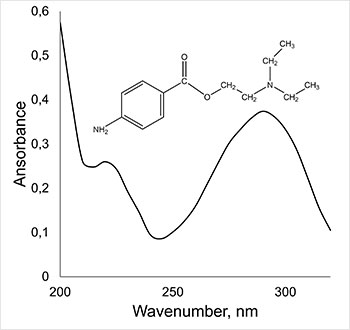
4-амінобензоату (анеститик прокаїн)
Якщо структура змінюється, наприклад, з’являється додатковий подвійний зв’язок – спектр також змінюється. Наявність хромофорів і ступінь їх спряження безпосередньо впливають на положення максимумів поглинання. Чим більш розвинена система спряжених подвійних зв’язків, тим легше електронам переходити на вищий енергетичний рівень, а отже, максимум поглинання зміщується в довгохвильову ділянку – відбувається батохромний зсув. Навпаки, руйнування спряження або поява замісників, що «відтягують» електронну густину, може спричиняти гіпсохромний зсув – переміщення максимуму в короткохвильову область. Такі зміни є інформативними під час порівняння споріднених сполук, контролю перебігу реакції або підтвердження модифікації структури.
Аналізуючи спектри за довідковими таблицями та використовуючи кількісні закономірності (зокрема закон Бугера–Ламберта–Бера), хімік може не лише зробити висновки про характер електронної системи молекули, а й визначити концентрацію речовини в розчині. Саме тому УФ-спектроскопія широко застосовується в фармацевтичному аналізі, біохімії та дослідженні біологічно активних сполук. Водночас цей метод практично неінформативний для насичених вуглеводнів і молекул без хромофорів, оскільки вони не мають електронних переходів у доступному спектральному діапазоні.
Інфрачервона спектроскопія: функціональні групи та структурні ознаки
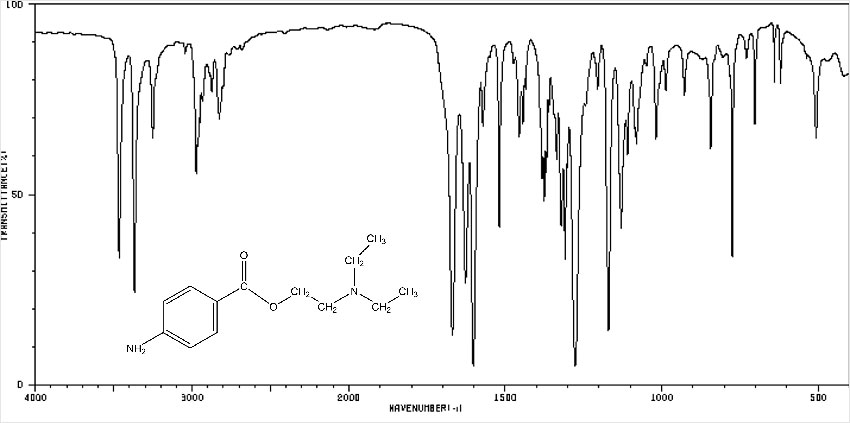
Інфрачервона спектроскопія (ІЧ) ставить молекулі інше запитання. Вона не «дивиться» на електрони, а спостерігає за коливаннями хімічних зв’язків. Атоми в молекулі не є нерухомими, вони постійно коливаються відносно один одного. Кожен тип зв’язку має власну характерну частоту коливань, а отже, поглинає інфрачервоне випромінювання в певному діапазоні, яке відповідає коливальним переходам у молекулі. Саме тому ІЧ-спектр дозволяє визначити наявність функціональних груп (наприклад, карбонільної, гідроксильної, амінної, тощо) та зв’язків між атомами. Для органічної хімії це надзвичайно цінна інформація, адже функціональна група визначає хімічні властивості сполуки.
Окрема частина ІЧ-спектра, відома як область «відбитків пальців», отримала свою назву завдяки своїй унікальності. У цій ділянці проявляються численні складні коливання каркаса молекули і сукупність цих смуг формує унікальний спектральний «візерунок», характерний саме для конкретної органічної сполуки, подібно до того, як відбитки пальців є унікальними для людини. Саме тому цю область активно використовують не лише для встановлення структури, а й для підтвердження ідентичності речовин у фармацевтичному контролі, аналітичній хімії та під час перевірки чистоти зразків. Принцип такого підтвердження достатньо простий: спектр досліджуваної сполуки порівнюють зі спектром еталонного зразка, записаним за однакових умов (тип пробопідготовки, розчинник або матриця, концентрація, температура). Якщо положення та інтенсивності основних смуг збігаються, це є переконливим аргументом на користь ідентичності. Виявлення додаткових смуг або змін їх форми може свідчити про наявність домішок або іншу структуру.
Водночас інтерпретація ІЧ-спектрів потребує обережності. У цій області часто спостерігається перекривання сигналів, а міжмолекулярні взаємодії, зокрема водневі зв’язки, можуть зміщувати або розширювати смуги поглинання. На положення піків також впливають агрегатний стан, природа розчинника та концентрація. Крім того, ІЧ-спектроскопія добре ідентифікує функціональні групи, але не дає повної інформації про взаємне розташування атомів у складному органічному каркасі. Тому в сучасній практиці її розглядають як важливий елемент комплексного структурного аналізу, який набуває максимальної інформативності у поєднанні з іншими методами.
ЯМР-спектроскопія: логіка структури і молекулярний контекст
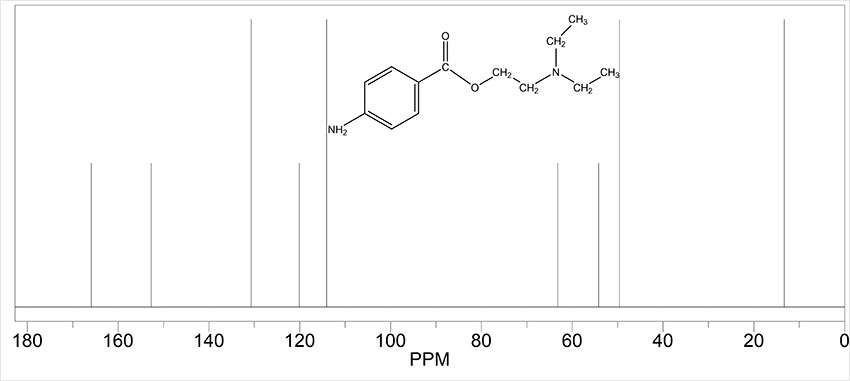
Спектроскопія ядерного магнітного резонансу (ЯМР) є одним із найінформативніших та найпотужніших методів дослідження органічних сполук. На перший погляд вона здається складною, адже пов’язана з магнітними властивостями атомних ядер та потребує потужних надпровідних магнітів. Проте її фізична ідея досить логічна. Деякі атомні ядра, наприклад, Гідрогену (¹H) та ізотопу Карбону ¹³C, мають власний ядерний спін і поводяться як крихітні магніти. Якщо помістити молекулу з такими атомами в сильне зовнішнє магнітне поле, ці «мікромагніти» можуть змінювати свій стан під дією випромінювання. Енергія такого переходу залежить від того, яке електронне оточення має конкретне ядро. Саме реєструючи ці енергетичні відмінності, хіміки отримують ЯМР-спектр.
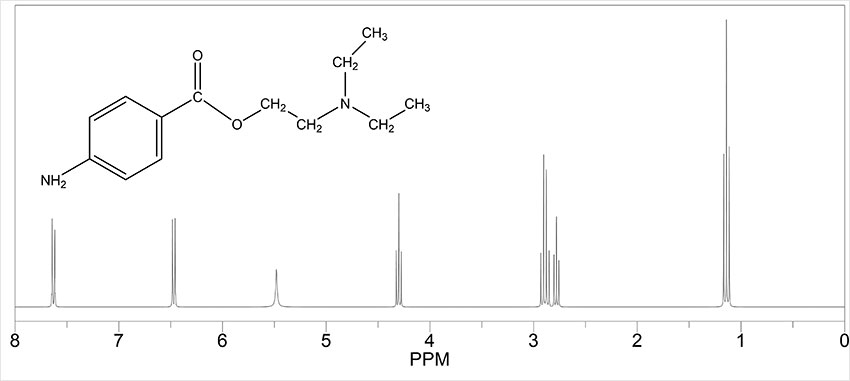
Особливо цінним для органічної хімії є те, що атоми Гідрогену в молекулі майже ніколи не є повністю однаковими. Один може бути приєднаний до карбонільної групи, інший входити до складу ароматичного кільця, третій – належати метильному фрагменту. Електронна густина навколо кожного з них різна, а отже, вони по-різному взаємодіють із зовнішнім магнітним полем, що відображається в положенні сигналу на спектрі. Таким чином, ¹H ЯМР-спектр показує, скільки типів протонів є в молекулі, у якому хімічному середовищі вони перебувають і навіть як вони взаємодіють із сусідніми атомами. Додаткова інформація про розщеплення сигналів (спін-спінову взаємодію) дозволяє встановити кількість сусідніх протонів, а інтегральна інтенсивність сигналів їх відносну кількість. Фактично це дає можливість «зчитати» фрагменти молекулярного каркаса.
Аналогічний підхід застосовується і для дослідження атомів Карбону. У ¹³C ЯМР-спектроскопії реєструються сигнали лише ізотопу ¹³C, який на відміну від надзвичайно поширеного ¹H становить лише приблизно 1,1 % всіх атомів Карбону у світі. Попри це, метод надзвичайно інформативний: він дозволяє аналогічно до ¹Н ЯМР визначити кількість нееквівалентних атомів Карбону в молекулі та оцінити їх оточення. У поєднанні ¹H та ¹³C ЯМР, а також спеціалізованих методик, можна практично повністю реконструювати каркас навіть дуже складної органічної сполуки.
Водночас ЯМР-спектроскопія має й певні обмеження, найважливішим з яких є дороговартісне обладнання та складне технічне обслуговування, що робить метод набагато менш доступним, ніж УФ чи ІЧ. Крім того, інтерпретація спектрів може бути складною у випадку великих або гнучких молекул, де сигнали перекриваються, а також для сумішей без попереднього розділення, тому як і будь-який інший метод, ЯМР дає найнадійніші результати не ізольовано, а в поєднанні з іншими аналітичними підходами.
Мас-спектрометрія: молекулярна маса та фрагментація
Ще одну ключову складову сучасного структурного аналізу органічних сполук забезпечує мас-спектрометрія – метод, який дає інформацію, недоступну жодному з класичних спектроскопічних підходів. Насамперед це точна молекулярна маса сполуки, яку за допомогою високороздільних приладів можна визначати з точністю до чотирьох знаків після коми. Така точність дозволяє встановити не лише масу, а й елементний склад молекули, розрізняючи формули, що відрізняються на частки атомної одиниці маси.
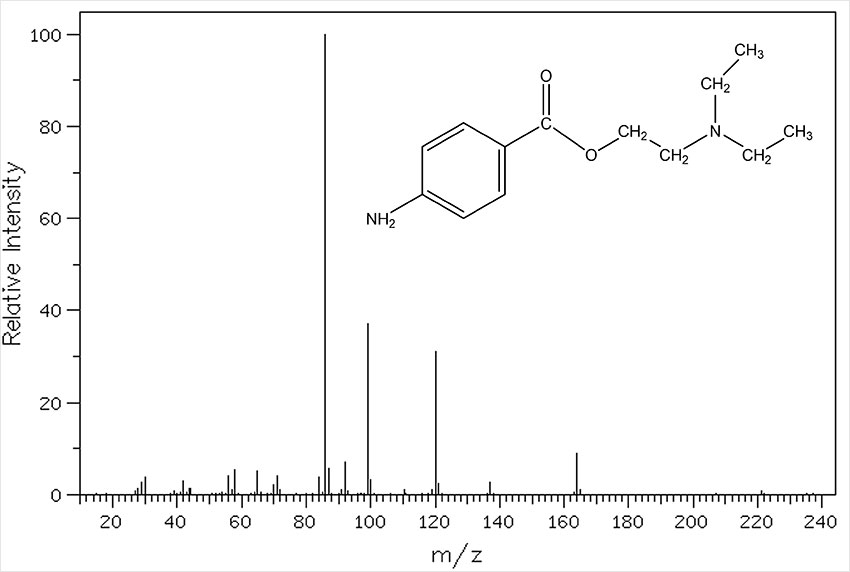
Принцип методу мас-спектрометрії полягає в тому, що молекули переводять у газову фазу та іонізують. Під час іонізації утворюється молекулярний іон – молекула, у якої «відірвали» електрон. Саме цей іон дозволяє визначити молекулярну масу. Далі він розпадається на фрагменти, а сукупність утворених іонів реєструється у вигляді мас-спектра. Такі спектри розглядаються як «карта фрагментації»: характерні шляхи розпаду багато в чому залежать від будови органічної сполуки, наявності функціональних груп та стабільності утворених іонів. Для органічної хімії це має особливе значення, бо в поєднанні з даними ЯМР та ІЧ, мас-спектрометрія суттєво звужує коло можливих структур та, наприклад, допомагає підтвердити правильність синтезу.
Особливо потужним є поєднання мас-спектрометрії з газовою та рідинною хроматографією. У таких системах спочатку відбувається розділення суміші на окремі компоненти, а потім кожен із них ідентифікується за мас-спектром. Це стандарт сучасного фармацевтичного контролю, токсикологічного аналізу, біоаналітики та дослідження природних сполук.
Водночас мас-спектрометрія має і певні обмеження. Не всі сполуки легко переходять у газову фазу, що є обов’язковою умовою для дослідження, або нестабільно іонізуються. Інколи молекулярний іон так швидко і повноцінно фрагментується, що може бути відсутнім на спектрі або дуже слабким. Крім того метод не дає прямої інформації про просторову будову молекули, тому зазвичай потребує підтвердження іншими аналітичними підходами. Крім того, високороздільні мас-спектрометри є складними й дорогими приладами.
Завдяки десятиліттям співпраці фізиків і хіміків сучасна наука отримала потужний інструментарій, що дозволяє впевнено відповідати на фундаментальні запитання: з яких атомів складається речовина, які зв’язки їх поєднують і як саме вибудуваний її молекулярний каркас. Те, що ще століття тому було предметом гіпотез, сьогодні підтверджується точними вимірюваннями.
Водночас жоден із методів не дає вичерпної відповіді на запитання «що це за молекула?». УФ-спектроскопія розкриває особливості електронної будови, ІЧ-аналіз дозволяє ідентифікувати функціональні групи, ЯМР відтворює логіку з’єднання атомів, а мас-спектрометрія встановлює молекулярну масу та характер фрагментації. Лише поєднання цих підходів перетворює набір сигналів на структурний доказ. Саме так у реальних лабораторіях встановлюють будову нових органічних сполук, перевіряють чистоту продуктів синтезу та контролюють якість фармацевтичних препаратів.

Список використаних джерел
- Аналітичні методи досліджень. Спектроскопічні методи аналізу: теоретичні основи і методики: навчальний посібник для підготовки студентів вищих навчальних закладів / Д.О. Мельничук, С.Д. Мельничук, В.М. Войціцький та ін.: за ред. акад. Д.О. Мельничука. – К.: ЦП «Компринт», 2016. – 289 с.
- Москаленко О. В., Циганков С. А., Янченко В. О., Циганков А. С. Спектральні методи аналізу. Ніжин: Видавництво НДУ імені Миколи Гоголя, 2022. 276 с.
- Stuart B. H. Infrared Spectroscopy: Fundamentals and Applications / Stuart. – Bremen: Wiley, 2014. – P. 244.
- Determination of enantiomeric purity and absolute configuration by NMR spectroscopy // Stereoselective Synthesis of Drugs and Natural Products, John Wiley & Sons, Inc. 2013.
- Elemental Analysis of Organic Species with Electron Ionization High-Resolution Mass Spectrometry / Aiken, Peter F. DeCarlo, Jose L. Jimenez // - Analytical Chemistry, Vol. 79, No. 21. - 2007.
Аліна Сікач, Національний університет «Києво-Могилянська Академія»




















 Засновник та видавець
Засновник та видавець