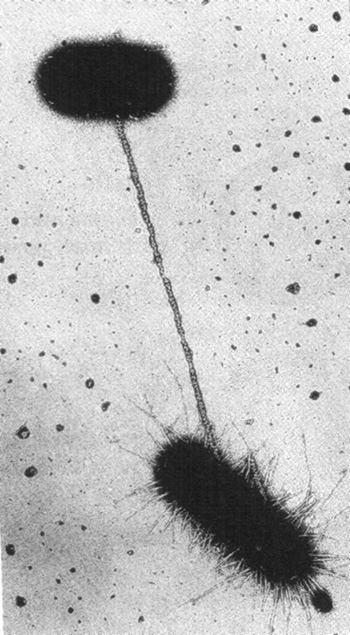
кишкової палочки E.coli,
з’єднаних виростом-трубочкою, по якому
генетична інформація від одної бактерії
переходить до другої.
Світ бактерій невидимий для людського ока. Без мікроскопа людина не може бачити бактерію, але повсюди може бачити результати життєдіяльності бактерій. У природі існує багато видів бактерій. Одні з них приносять користь людині, а інші викликають ряд захворювань. Всі бактерії, як і все живе на нашій планеті, постійно ведуть боротьбу за виживання, пристосовуючись до тих чи інших умов оточуючого середовища, а також постійно «воюючи» з іншими бактеріями за життєвий простір, використовуючи різного плану «молекулярну зброю». Саме ця «молекулярна зброя» і складає нині основний арсенал молекулярно-біологічних «інструментів», без яких сучасна молекулярна біологія не могла б існувати. Це, переважно, плазміди та рестрикційні ферменти. Про них і піде мова далі.
Бактерії, як і інші одноклітинні живі істоти, мають набір генів, необхідний для відтворення собі подібних організмів. Ці гени знаходяться в молекулі бактеріальної ДНК, яка утворює хромосомо-подібну структуру і локалізується в цитоплазмі, бо клітинного ядра бактерії не мають. Надзвичайно важливою особливістю бактеріального світу є наявність в них особливої позахромосомної ДНК, яка має відносно невеликий розмір і називається плазмідою. Зараз відомо багато класів плазмід з різними властивостями, але всі вони здатні до самореплікації, тобто здатні самі себе відтворювати незалежно від реплікації хромосомної ДНК. Це своєрідна форма збереження спадкової інформації, а також переносу та рекомбінації генів, що має надзвичайно важливе значення для виживання бактерій.
Саме плазміди є тими структурами бактерій, які є тотожними факторам плодючості бактерій, вони також детермінують стійкість бактерій до лікарських препаратів (антибіотиків, зокрема), що і забезпечує виживання бактерій в несприятливих умовах. Плазміди – це створені самою природою моделі для генетичних та молекулярно-біологічних експериментів. Плазміди – це один із видів «захисту» бактерій, з одного боку, і «зброї» бактерій, з іншого боку. Стійкість бактерій до лікарських препаратів є надзвичайно важливою проблемою для медицини, а для бактерій це спосіб захистити себе і вижити в присутності токсичних для них речовин. Ця стійкість забезпечується наявністю в бактеріях певного класу плазмід, що містять гени стійкості до одного або декількох антибіотиків. Бактерії, що мають такі плазміди, не гинуть від антибіотика (антибіотиків), вони живуть і розмножуються в його (їх) присутності. У даному випадку плазміди забезпечують «захист» бактерій. Разом з тим, є плазміди, що містять гени для синтезу токсинів. Бактерії, що мають таку плазміду, синтезують і виділяють у середовище токсини, що вбивають інших бактерій. У цьому випадку плазміди виробляють «молекулярну зброю», яка діє проти інших бактерій.
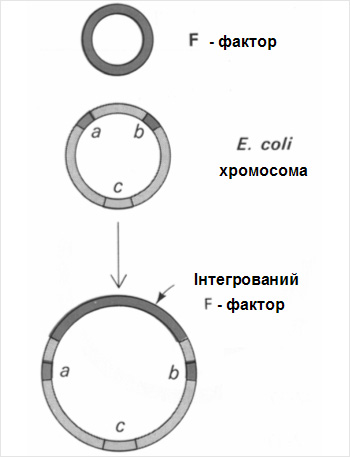
інформація (F- фактор), попавши в бактерію,
вбудовується в її хромосому.
Яким чином появляється стійкість до одного або декількох антибіотиків у бактерій, які були чутливими до антибіотиків? Чутливі до антибіотика бактерії не мають плазміди з геном стійкості до даного антибіотика і в присутності антибіотика гинуть, але в цих екстремальних умовах мізерна кількість бактерій може захопити таку плазміду від іншого виду бактерій, часто сапрофітних, і таким чином «захистити» себе від загибелі. Саме обмін плазмідами між бактеріями забезпечує їх пристосування до змінених умов існування і, зокрема, дає можливість бактеріям рости в присутності антибіотика. Більше того, ці плазміди здатні до перебудов й інколи включають у себе додаткові гени, зокрема, гени стійкості до ряду інших антибіотикам, що і визначає явище мультирезистентності, коли на бактерії не діє не один, а одночасно декілька антибіотиків.
Захоплюючи плазміди з генами для синтезу токсинів, бактерії стають «воїнами». Плазміди є динамічними структурами і здатні змінювати закодовану в них генетичну інформацію, включаючи не лише нові, додаткові гени, а навіть і оперони, але разом з тим можуть також і втрачати гени. Ці унікальні властивості плазмід і використовують молекулярні біологи та молекулярні біотехнологи для клонування різних генів у плазмідах та експресії їх в бактеріях. Для клонування генів необхідно розрізати плазмідну ДНК і вставити ген. Але розрізати треба лише в одному, певному місці і до цих кінців пришити ген, який ми хочемо вставити і клонувати. Як було сказано вище, бактерії вміють це робити, вставляють і викидають гени чи групи генів із плазмід в залежності від потреб, і мають необхідні для цього «інструменти» (ферменти).
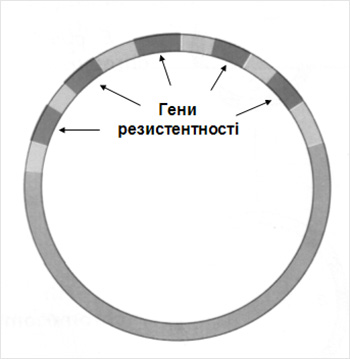
бактерій до антибіотиків. Темним тоном
позначені гени резистентності.
Молекулярними ножицями, що розрізають ДНК лише в певних місцях, а інколи лише в одному місці на всю плазмідну ДНК, є рестрикційні ферменти (рестрикційні ендонуклеази або рестриктази). Це сильна «молекулярна зброя», за допомогою якої одні бактерії можуть вбивати інших, розрізаючи і таким чином руйнуючи хромосомну ДНК. Розрізання ДНК, або рестрикція, проходить по певним нуклеотидним послідовностям, які можна розділити на дві симетричних частини.
Є рестрикційні ферменти, що впізнають одну і ту ж послідовність нуклеотидів, але по-різному її розрізають або мають різні властивості. Ця «молекулярна зброя» виробляється для знищення інших бактерій і не діє на ДНК бактерії-хазяїна. Яким же чином бактерія-хазяїн захищає свою ДНК? Головним чином це забезпечується унікальним механізмом модифікації нуклеотидних послідовностей, які розпізнаються даною рестриктазою, за рахунок метилування певних нуклеотидів цих послідовностей специфічними ферментами або самими рестриктазами, якщо вони мають подвійну ферментативну активність: для рестрикції і для метилування. Таким чином, вся ДНК бактерії-«воїна», що виробляє «молекулярну зброю», захищена від неї специфічним метилуванням тих нуклеотидних послідовностей, що розпізнаються рестриктазами.
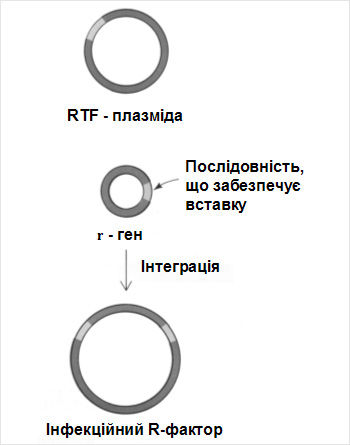
шляхом інтеграції в плазміди генів
інфекційності.
Ця «молекулярна зброя» знайшла широке використання в молекулярній біології не лише для клонування генів, а і для аналізу та вивчення структури ДНК. Іншим «інструментом», без якого не можливе клонування, є ферменти лігази, які зшивають розрізані ділянки ДНК, але не всі, а лише певні. Пов’язано це з тим, що різні рестриктази по-різному розрізають ДНК, створюючи відмінні по своїй структурі кінці. Якщо ДНК розрізається одним рестрикційним ферментом, то утворені при цьому кінці легко зшиваються. Якщо до такої ДНК додати фрагмент іншої ДНК чи ген, вирізаний цим же ферментом, то лігаза дуже легко зшиває такі кінці ДНК. У тому випадку, коли ДНК розрізається різними рестриктазами, то кінці здебільшого відрізняються і не можуть зшиватися лігазами.
Таким чином, бактеріальний світ є надзвичайно складним і цікавим з надзвичайно досконалими способами боротьби за виживання. Пізнання лише деяких сторін життєдіяльності бактерій протягом останніх десятиліть створило міцний фундамент для нової науки – молекулярної біології, для пізнання структури і функції геному людини та багатьох інших організмів та розвитку молекулярних біотехнологій. Молекулярна біологія дала можливість створити генно-інженерним способом багато ліків (рекомбінантні гормони людини: інсулін, гормон росту та інші) та розпочати генотерапію.
О. Г. Мінченко доктор біологічних наук, Інституту біохімії НАН України












![Невичерпні проблеми природи світла [2]](/images/202603/light.jpg#joomlaImage://local-images/202603/light.jpg?width=850&height=587)



 Засновник та видавець
Засновник та видавець